Mesin Carnot adalah mesin kalor hipotetis yang beroperasi dalam suatu siklus reversibel yang disebut siklus Carnot. Model dasar mesin ini dirancang oleh Nicolas Léonard Sadi Carnot, seorang insinyur militer Perancis pada tahun 1824. Model mesin Carnot kemudian dikembangkan secara grafis oleh Émile Clapeyron 1834, dan diuraikan secara matematis oleh Rudolf Clausius pada 1850an dan 1860an. Dari pengembangan Clausius dan Clapeyron inilah konsep dari entropi mulai muncul.
Mesin Carnot adalah mesin kalor hipotetis yang beroperasi dalam suatu siklus reversibel yang disebut siklus Carnot. Model dasar mesin ini dirancang oleh Nicolas Léonard Sadi Carnot, seorang insinyur militer Perancis pada tahun 1824. Model mesin Carnot kemudian dikembangkan secara grafis oleh Émile Clapeyron 1834, dan diuraikan secara matematis oleh Rudolf Clausius pada 1850an dan 1860an. Dari pengembangan Clausius dan Clapeyron inilah konsep dari entropi mulai muncul.
Setiap sistem termodinamika berada dalam keadaan tertentu. Sebuah siklus termodinamika terjadi ketika suatu sistem mengalami rangkaian keadaan-keadaan yang berbeda, dan akhirnya kembali ke keadaan semula. Dalam proses melalui siklus ini, sistem tersebut dapat melakukan usaha terhadap lingkungannya, sehingga disebut mesin kalor.
Sebuah mesin kalor bekerja dengan cara memindahkan energi dari daerah yang lebih panas ke daerah yang lebih dingin, dan dalam prosesnya, mengubah sebagian energi menjadi usaha mekanis. Sistem yang bekerja sebaliknya, dimana gaya eksternal yang dikerjakan pada suatu mesin kalor dapat menyebabkan proses yang memindahkan energi panas dari daerah yang lebih dingin ke energi panas disebut mesin refrigerator.
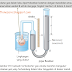
Pada diagram di samping, yang diperoleh dari tulisan Sadi Carnot berjudul Pemikiran tentang Daya Penggerak dari Api (Réflexions sur la Puissance Motrice du Feu), diilustrasikan ada dua benda A dan B, yang temperaturnya dijaga selalu tetap, dimana A memiliki temperatur lebih tinggi daripada B. Kita dapat memberikan atau melepaskan kalor pada atau dari kedua benda ini tanpa mengubah suhunya, dan bertindak sebagai dua reservoir kalor. Carnot menyebut benda A "tungku" dan benda B "kulkas".Carnot lalu menjelaskan bagaimana kita bisa memperoleh daya penggerak (usaha), dengan cara memindahkan sejumlah tertentu kalor dari reservoir A ke B.
Diagram modern
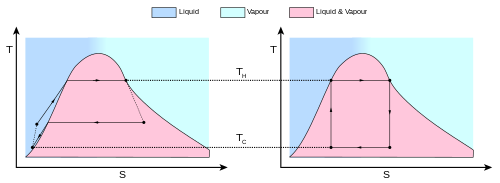
Dibawah ini adalah diagram mesin Carnot sebagaimana biasanya dimodelkan dalam pembahasan modern
Diagram mesin Carnot (modern) - kalor mengalir dari reservoir bersuhu tinggi THmelalui "fluida kerja", menuju reservoir dingin TC, dan menyebabkan fluida kerja memberikan usaha mekanis kepada lingkungan, melalui siklus penyusutan (kontraksi) dan pemuaian (ekspansi).
Dalam diagram tersebut, sistem ("fluida kerja"), dapat berupa benda fluida atau uap apapun yang dapat menerima dan memancarkan kalor Q, untuk menghasilkan usaha. Carnot mengusulkan bahwa fluida ini dapat berupa zat apapun yang dapat mengalami ekspansi, seperti uap air, uap alkohol, uap raksa, gas permanen, udara, dll. Sekalipun begitu, pada tahun-tahun awal, mesin-mesin kalor biasanya memiliki beberapa konfigurasi khusus, yaitu QH disuplai oleh pendidih, di mana air didihkan pada sebuah tungku, QCbiasanya adalah aliran air dingin dalam bentuk embun yang terletak di berbagai bagian mesin. Usaha keluaran W biasanya adalah gerakan piston yang digunakan untuk memutar sebuah engkol, yang selanjutnya digunakan untuk memutar sebuah katrol. Penggunaannya biasanya untuk mengangkut air dari sebuah pertambangan garam. Carnot sendiri mendefinisikan "usaha" sebagai "berat yang diangkat melalui sebuah ketinggian".
Teorema Carnot
Sebuah mesin nyata (real) yang beroperasi dalam suatu siklus pada temperatur 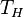 and
and 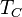 tidak mungkin melebihi efisiensi mesin Carnot.
tidak mungkin melebihi efisiensi mesin Carnot.
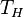 and
and  tidak mungkin melebihi efisiensi mesin Carnot.
tidak mungkin melebihi efisiensi mesin Carnot.
Teorema Carnot adalah pernyataan formal dari fakta bahwa: Tidak mungkin ada mesin yang beroperasi di antara dua reservoir panas yang lebih efisien daripada sebuah mesin Carnot yang beroperasi pada dua reservoir yang sama. Artinya, efisiensi maksimum yang dimungkinkan untuk sebuah mesin yang menggunakan temperatur tertentu diberikan oleh efisiensi mesin Carnot,
Implikasi lain dari teorema Carnot adalah mesin reversibel yang beroperasi antara dua reservoir panas yang sama memiliki efisiensi yang sama pula.
Efisiensi maksimum yang dinyatakan pada persamaan diatas dapat diperoleh jika dan hanya jika tidak ada entropi yang diciptakan dalam siklus tersebut. Jika ada, maka karena entropi adalah fungsi keadaan, untuk membuang kelebihan entropi agar dapat kembali ke keadaan semula akan melibatkan pembuangan kalor ke lingkungan, yang merupakan proses irreversibel dan akan menyebabkan turunnya efisiensi. Jadi persamaan di atas hanya memberikan efisiensi dari sebuah mesin kalor reversibel.
Sumber:
- Kroemer, Herbert; Kittel, Charles (1980). Thermal Physics (ed. 2nd ed.). W. H. Freeman Company. ISBN 0-7167-1088-9.
- ^ Carnot, Sadi (1824). Réflexions sur la Puissance Motrice du Feu, page 17.












 Silahkan download
Silahkan download